La aleatorización es un pilar fundamental en la realización de ensayos clínicos modernos. Este proceso, que consiste en asignar aleatoriamente a los participantes a diferentes grupos de intervención y control, desempeña un papel crucial en la obtención de resultados fiables y generalizables.
Al equilibrar las características conocidas y desconocidas de los pacientes entre los grupos, la aleatorización reduce el riesgo de sesgo de selección que podría distorsionar la interpretación del efecto de un tratamiento. En un ensayo clínico, esta técnica garantiza que cada paciente tenga las mismas probabilidades de ser asignado a cualquier grupo, ya sea el tratamiento experimental, un placebo o el tratamiento estándar.
Los ensayos clínicos aleatorizados se consideran el estándar de referencia para la evaluación terapéutica, proporcionando a investigadores y clínicos evidencia sólida en la que basar las decisiones médicas.
¿Por qué es importante la aleatorización en la investigación clínica?
La aleatorización es esencial en la investigación clínica porque garantiza la equidad en la distribución de participantes y minimiza los sesgos. Permite una comparación objetiva y científica de los efectos del tratamiento.
Esta asignación aleatoria es crucial para la validez de un estudio clínico. Ayuda a equilibrar los factores pronósticos conocidos y desconocidos entre los grupos, facilitando la atribución de las diferencias observadas al tratamiento estudiado en lugar de a las características preexistentes de los pacientes.
En la práctica, la aleatorización también facilita el enmascaramiento de los estudios (simple o doble ciego), donde ni los participantes ni, en algunos casos, los investigadores saben qué tratamiento se ha asignado, reforzando aún más el rigor metodológico del ensayo.
Métodos de aleatorización en ensayos clínicos
Generación de listas
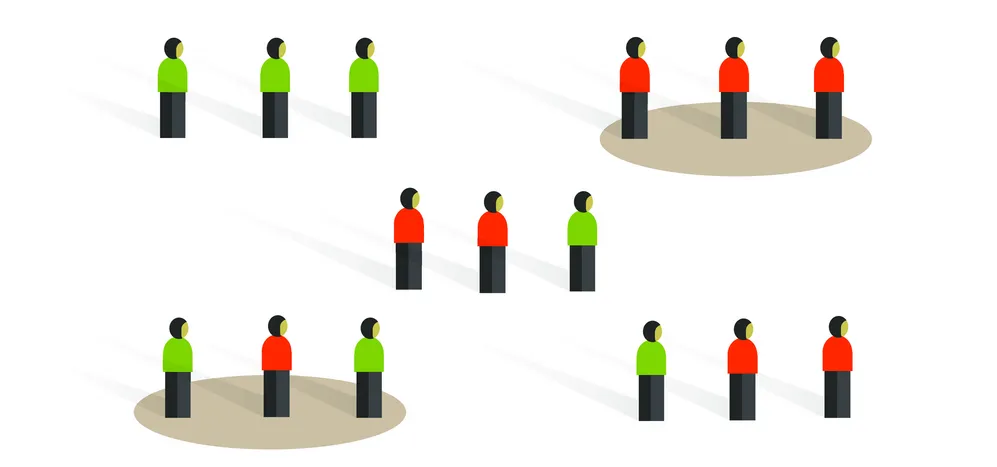
- Aleatorización por bloques
Los participantes se dividen en bloques fijos o variables para garantizar un número equilibrado en cada grupo. Esta técnica divide a los participantes en bloques de tamaño fijo, garantizando el equilibrio numérico a intervalos regulares. Por ejemplo, en un bloque de 4, dos serán asignados al tratamiento experimental y dos al control, con el orden de asignación aleatorizado dentro del bloque. - Aleatorización adaptativa o dinámica
Los participantes se asignan en función de probabilidades de asignación determinadas por sus características. Este enfoque busca optimizar el equilibrio entre los grupos a lo largo del estudio.
Métodos de distribución
- Aleatorización simple
Los participantes se asignan aleatoriamente sin ninguna estratificación. Este método, similar a un sorteo, es fácil de implementar pero puede generar desequilibrios entre los grupos, especialmente en estudios con muestras pequeñas. - Aleatorización estratificada
Los participantes se estratifican primero según ciertas características (edad, sexo, etc.) antes de ser aleatorizados. Cuando las características de los pacientes pueden influir significativamente en los resultados, este método resulta valioso, ya que garantiza una distribución equitativa de los factores pronósticos importantes entre los grupos de intervención y control. - Aleatorización por conglomerados
En algunos ensayos clínicos, se aleatorizan grupos enteros (como hospitales, pueblos o escuelas) en lugar de individuos. Este enfoque se utiliza cuando el tratamiento debe aplicarse a toda una comunidad, o cuando existe riesgo de "contaminación" entre participantes individuales.
Condiciones del estudio
- Aleatorización simple ciego
En un estudio simple ciego, los participantes no saben qué tratamiento reciben, pero los investigadores sí. - Aleatorización doble ciego
En un estudio doble ciego, ni los participantes ni los investigadores saben quién recibe qué tratamiento. Esto elimina tanto los sesgos conscientes como los inconscientes.
¿Cuáles son las ventajas y desventajas de la aleatorización?
Ventajas de la aleatorización en ensayos clínicos
La aleatorización ofrece varias ventajas decisivas para la validez de los ensayos clínicos:
- Reducción de sesgos: Minimiza el riesgo de que los resultados estén influenciados por factores distintos a la intervención estudiada.
- Equilibrio de variables pronósticas: Las características que podrían afectar la progresión de la enfermedad se distribuyen equitativamente entre los grupos.
- Base estadística sólida: La aleatorización permite el uso de pruebas estadísticas válidas para analizar los resultados del ensayo.
- Mayor credibilidad: Los controles aleatorizados se consideran el nivel más alto de evidencia científica, aumentando la confianza en los efectos observados del tratamiento.
Beneficios clave de la aleatorización en sistemas eCRF/EDC:
La aleatorización integrada en las plataformas eCRF/EDC reduce considerablemente el error humano mediante la automatización de procesos, garantiza una documentación precisa y completa con una pista de auditoría verificable, y optimiza significativamente los flujos de trabajo clínicos al permitir que los investigadores aleatoricen a los pacientes en unos pocos clics. Esto refuerza la integridad científica y acelera la ejecución del ensayo. Un sistema EDC elimina todas las limitaciones logísticas de asignación y gestión entre centros, equipos, idiomas y zonas horarias, permitiendo una aleatorización equilibrada a nivel global, un desafío importante en los estudios multicéntricos.
Riesgos y desafíos de la aleatorización
Una aleatorización inadecuada puede introducir sesgos sistemáticos en un estudio. Por ejemplo, si la secuencia de aleatorización es predecible o la asignación no se oculta correctamente, los investigadores podrían (consciente o inconscientemente) influir en la asignación de los pacientes.
El tamaño de la muestra también desempeña un papel crucial. En ensayos pequeños, incluso una aleatorización correctamente ejecutada puede generar grupos desequilibrados por simple azar, comprometiendo potencialmente la validez del análisis.
Además, algunos participantes pueden negarse a participar en un estudio si no se les garantiza recibir el tratamiento experimental, lo que puede afectar la representatividad de la muestra y la generalización de los resultados.
Más información sobre la aleatorización
Cómo preparar un protocolo de estudio que integre la aleatorización
Preparar un protocolo de estudio con aleatorización requiere considerar cuidadosamente varios elementos clave:
- Elegir las condiciones de asignación y seguimiento adecuadas a los objetivos del estudio y las características de los pacientes
- Determinar el tamaño de muestra necesario para detectar el efecto esperado del tratamiento
- Diseñar el proceso de ocultación de la asignación
- Planificar los análisis estadísticos apropiados para evaluar los resultados del ensayo
Un protocolo bien diseñado debe anticipar los posibles desafíos y proporcionar mecanismos para mantener la integridad del proceso de aleatorización a lo largo del ensayo clínico.











.webp)
.webp)
