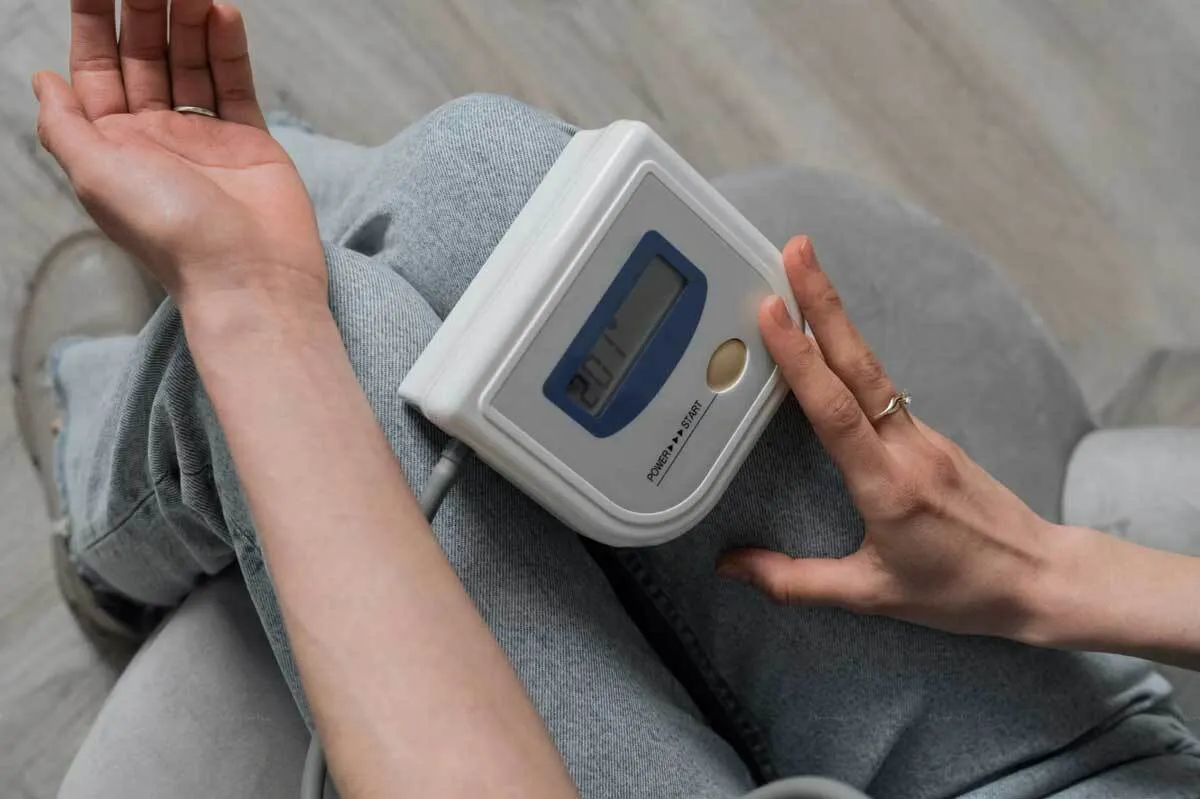
Réglementations EU MDR : Mise en œuvre de plans de surveillance post-commercialisation (PMS) et d’études post-market clinical follow-up (PMCF) pour les fabricants de dispositifs médicaux.
Les fabricants de dispositifs médicaux doivent se conformer à la nouvelle réglementation EU MDR, qui requiert la mise en place d’études PMS (Post-Market Surveillance) et PMCF (Post-Market Clinical Follow-up).
Il est important de noter que la réglementation n’impose pas de format spécifique pour la réalisation de ces études PMS/PMCF. Vous avez plusieurs options à votre disposition : vous pouvez mener des études cliniques traditionnelles, utiliser des ressources documentaires et scientifiques, ou encore mener des enquêtes auprès de professionnels de santé ou de patients. Cette diversité d’approches peut sembler complexe, c’est pourquoi il est essentiel de choisir soigneusement les bons outils et partenaires pour mener à bien vos études PMCF.
Pourquoi utiliser une plateforme eCRF pour mes études en PMCF ?
1. Une collecte de données efficace
Une solution eCRF vous permet de collecter et de saisir facilement les données pertinentes pour vos études PMCF. Vous pouvez créer des formulaires électroniques personnalisés pour recueillir les informations spécifiques dont vous avez besoin. Cela élimine les tâches fastidieuses de saisie manuelle des données à partir de documents papier ou de feuilles de calcul Excel, ce qui vous fait gagner du temps et réduit les erreurs potentielles.
2. Des données de qualité
Utiliser une plateforme eCRF vous permettra d’améliorer l’exactitude des données collectées en réduisant les erreurs de retranscription, les données manquantes ou surprenantes, en soulevant des requêtes automatiques sur vos formulaires. La plateforme fournit des validations de données en temps-réel, et alertes en cas d’erreurs potentielles
3. Conformité accrue
Les solutions EDC offrent un stockage sécurisé des données dans le cloud, ce qui garantit la protection et la confidentialité des informations collectées. Vous pouvez définir des autorisations d’accès pour contrôler qui peut consulter et modifier les données, assurant ainsi la conformité aux normes de protection des données (ISO 27001, ICH GCP, FDA 21 CFR Part 11, RGPD…).
4. Accès rapide et centralisé aux données
Grâce à une solution eCRF, vous pouvez accéder rapidement à l’ensemble de vos données PMCF à partir d’un emplacement centralisé. Cela facilite la gestion et l’analyse des données, vous permettant de prendre des décisions éclairées en temps réel. Vous pouvez également générer des rapports et des tableaux de bord pour visualiser les résultats et les tendances, ce qui facilite l’identification des problèmes potentiels et l’évaluation de l’efficacité de vos dispositifs médicaux.
5. Automatisation des tâches
Une solution eCRF peut automatiser certaines tâches liées à la collecte et à la gestion des données PMCF. Cela peut inclure des fonctionnalités telles que des alertes pour les données manquantes ou aberrantes, des rappels pour les visites de suivi, ou encore des calculs automatiques. Ces automatisations permettent de réduire les erreurs humaines et d’optimiser l’efficacité des processus.
6. L’analyse des données collectées
Utiliser un système eCRF vous apporte également une facilité d’export et d’analyse de vos données collectées. En effet, vous pouvez choisir vos formats d’exports (PDF, CSV, XLSX…). Vous pouvez également réaliser des analyses préliminaires directement sur le plateforme EDC en créant des tableaux et graphiques d’analyse de données ou en accédant à des rapports automatiques et des tableaux de bord.
7. Réduction des coûts
Une plateforme EDC vous permet de réduire drastiquement vos coûts d’études. En effet, son usage élimine l’ensemble de la logistique papier (papier, impression, encre, archivage…), de détecter les erreurs et les incohérences dès leur saisie. Cela réduit la nécessité de corrections ultérieures coûteuses et chronophages, telles que la recherche et la correction d’erreurs dans les formulaires papier.
De plus, toutes les données cliniques sont centralisées sur une seule et même plateforme, ce qui facilite les audits et les inspections réglementaires. Cela peut réduire les coûts associés à la préparation et à la gestion des audits, ainsi qu’à la recherche et à la récupération des documents papier nécessaires.
8. Meilleure Collaboration
Une solution eCRF facilite la collaboration au sein de l’équipe de recherche en offrant des fonctionnalités adaptées à chaque utilisateur de la plateforme, selon leurs autorisations spécifiques. Les membres de l’équipe peuvent saisir des données simultanément, ce qui favorise la communication et la coordination entre eux tout en réduisant les risques d’erreurs.
Grâce à des accès spécifiques, chaque membre peut contribuer efficacement aux études en entrant les données qui leur sont assignées, tout en respectant les rôles et les autorisations définis. Cela permet une répartition équilibrée des tâches et une meilleure synchronisation des activités de collecte de données.